เมื่อช่วงปลายอาทิตย์ที่แล้วมีข่าวใหญ่เมื่อบริษัท Pfizer-BioNTech ได้เปิดตัวยาเม็ดสำหรับรักษา COVID-19 ในชื่อ “Paxlovid” และที่น่าตื่นตาตื่นใจกว่านั้นก็เพราะประสิทธิภาพในการป้องกันเสียชีวิตและป่วยหนักของมันสูงเกือบ 90%
ขณะที่เมื่อช่วงต้นเดือนตุลาคมที่ผ่านมา Merck & Co. และ Ridgeback Biotherapeutics ก็ได้เปิดตัวยาเม็ดรักษา COVID-19 เช่นกันในชื่อ “Molnupiravir”
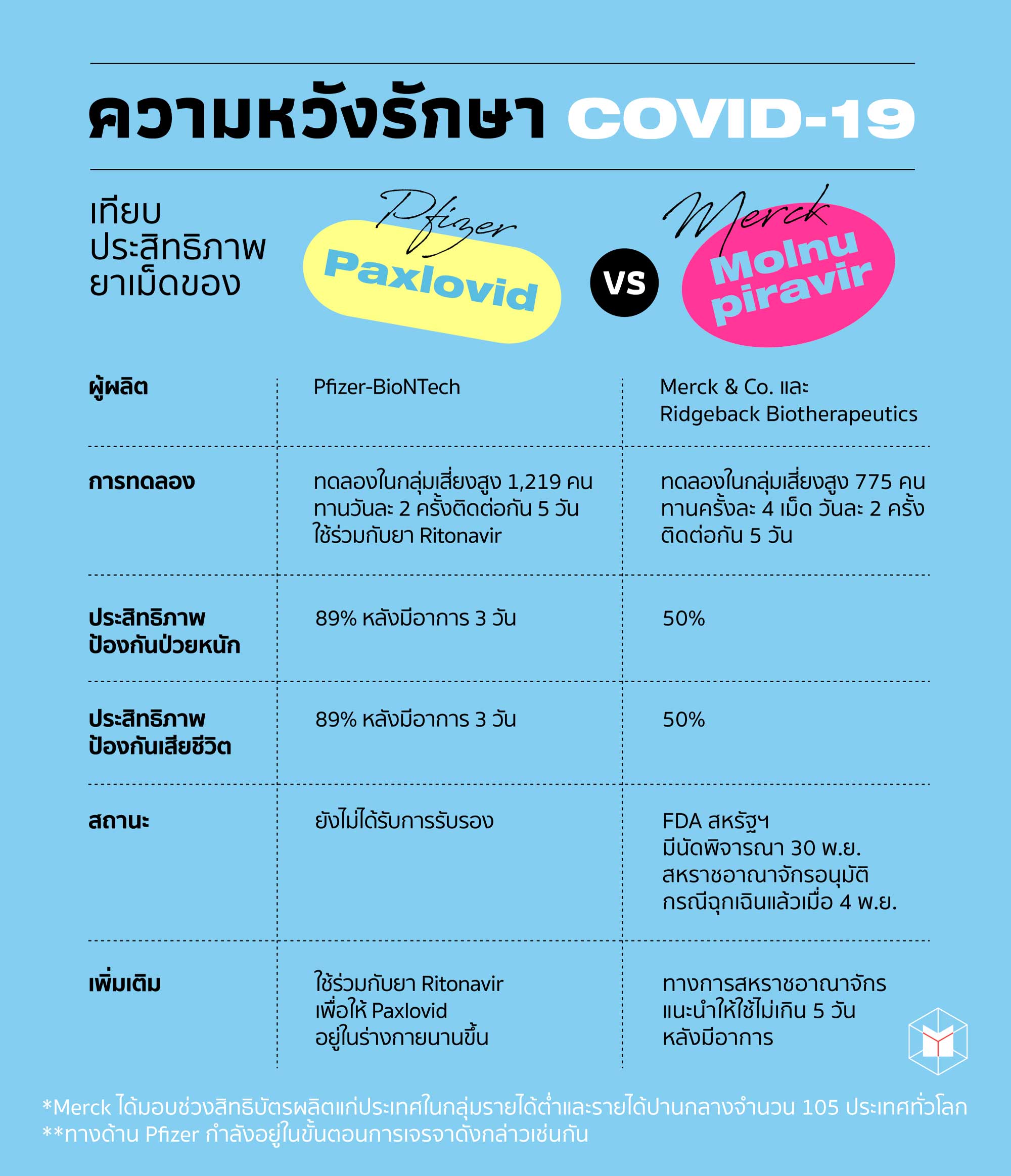
เมื่อยาเม็ดทั้งสองตัวถูกยกย่องว่าเป็น “ตัวเปลี่ยนเกมส์ (Game Changer)” จากสื่อหลายสำนัก วันนี้ The MATTER จึงยกยาทั้งสองชนิดมาเทียบให้ดูชนิดปอนด์ต่อปอนด์ หมัดต่อหมัดว่าตัวไหนมีผลการทดลองเป็นอย่างไรและประสิทธิภาพสูงแค่ไหน
Paxlovid
Paxlovid เป็นยาเม็ดที่ผลิตโดยบริษัท Pfizer-BioNTech หรือผู้ผลิตเดียวกับวัคซีน Pfizer นั่นเอง
โดยช่วงปลายอาทิตย์ที่แล้ว บริษัท Pfizer ได้เปิดเผยผลการศึกษาระยะที่ 2 ควบ 3 ของยา Paxlovid กับผู้ป่วยกลุ่มเสี่ยงสูงที่ติดเชื้อไวรัส COVID-19 จำนวน 1,219 คน โดยให้ทานครั้งละ 3 เม็ด (ใช้คู่กับยา Ritonavir เพื่อให้ Paxlovid มีประสิทธิภาพสูงขึ้น) วันละ 2 ครั้ง ติดต่อกัน 5 วัน หรือรวมเป็นทั้งหมด 30 เม็ดต่อการรักษาครั้งหนึ่ง
ผลการศึกษาที่ออกมาโดดเด่นมาก โดยสำหรับผู้ป่วยที่ได้รับยา Paxlovid ภายใน 3 วันที่เริ่มแสดงอาการของไวรัส COVID-19 มีเพียง 0.8% ที่ต้องเข้ารักษาตัวที่โรงพยาบาล และไม่มีผู้เสียชีวิต ขณะที่กลุ่มตัวอย่างที่ได้ยาปลอมมี 7% ที่ต้องเข้ารับการรักษาตัวในโรงพยาบาล และมีทั้งหมด 7 รายที่เสียชีวิต
ขณะที่ผลการทดลองให้ยาดังกล่าวกับผู้ป่วยที่มีอาการมาแล้ว 5 วัน พบว่ามี 1% ที่ต้องเข้ารักษาตัวที่โรงพยาบาล และไม่มีผู้เสียชีวิต ขณะที่กลุ่มที่ได้รับยาหลอกมี 6.7% ที่ต้องเข้ารักษาตัวที่โรงพยาบาล และมี 10 รายที่เสียชีวิต
จากผลการทดลองบริษัท Pfizer สรุปว่ายา Paxlovid มีประสิทธิภาพในการป้องกันอาการป่วยหนัก 89% และป้องกันเสียชีวิต 89%
มาถึงตอนนี้ยังไม่มีประเทศไหนประกาศรับรองยาชนิดดังกล่าว แต่มีข่าวว่าบริษัทกำลังเตรียมเอกสารเพื่อยื่นให้ FDA ของสหรัฐฯ ภายในวันที่ 25 พ.ย. นี้
Molnupiravir
สำหรับยา Molnupiravir ซึ่งตกเป็นข่าวครึกโครมเมื่อช่วงต้นเดือนตุลาคม เป็นผลงานความร่วมมือระหว่างบริษัท Merck & Co. และ Ridgeback Biotherapeutics
จากการทดลองระดับคลินิคในผู้ป่วยกลุ่มเสี่ยงสูงจำนวน 775 คน โดยให้รับประทานยา Molnupiravir วันละ 2 ครั้ง ติดต่อกัน 5 วัน
ผลจากการวิจัยพบว่าผู้ที่ได้รับยา Molnupiravir เป็นระยะเวลา 5 วัน มีเพียง 7.3% ของผู้ป่วยที่ต้องเข้ารับการรักษาตัวในโรงพยาบาล และไม่พบผู้เสียชีวิตตลอดการรักษา 29 วัน ขณะที่อีกกลุ่มหนึ่งซึ่งได้รับยาหลอกพบว่ามี 14.1% ที่ต้องเข้ารับการรักษาตัวในโรงพยาบาล และมีผู้เสียชีวิต 8 ราย
ดังนั้น ผลการทดลองสรุปว่ายา Molnupiravir มีประสิทธิภาพในการป้องกันอาการป่วยหนักและเสียชีวิตเท่ากันที่ 50% อย่างไรก็ตาม ข้อมูลจากการวิจัยชี้เพิ่มว่าควรให้ยานี้แก่ผู้ที่เพิ่งป่วยไม่เกิน 5 วันเพื่อให้มีประสิทธิภาพสูงสุด
ล่าสุดเมื่อวันที่ 4 พ.ย. ที่ผ่านมา ทางสหราชอาณาจักรได้ประกาศให้ใช้ยา Molnupiravir ในกรณีฉุกเฉินแล้ว โดยมีคำแนะนำแนบมาว่า “ต้องใช้ให้เร็วที่สุด (As Soon As Possible)” ขณะที่ทาง FDA ของสหรัฐฯ เตรียมพิจารณาให้ใช้ยาชนิดนี้ในกรณีฉุกเฉินในวันที่ 30 พ.ย. ที่จะถึงนี้
อีกหนึ่งข่าวดีคือ ผู้ผลิตยา Molnupiravir ได้มอบช่วงสิทธิบัตรผลิตแก่ประเทศในกลุ่มรายได้ต่ำและรายได้ปานกลางจำนวน 105 ประเทศทั่วโลก กล่าวคือถ้าการเจรจาสำเร็จ ประเทศรายได้ปานกลางและต่ำจะสามารถผลิต Molnupiravir ใช้ได้เองเลย ไม่จำเป็นต้องสั่งซื้อ ขณะที่ Paxlovid กำลังอยู่ในขั้นตอนเจรจาดังกล่าวเช่นกัน
แผนจัดซื้อของกระทรวงสาธารณสุข
ล่าสุดวันนี้ นพ.อรรถสิทธิ์ ศรีสุบัติ ที่ปรึกษากรมการแพทย์กระทรวงสาธารณสุขเพิ่งแถลงข่าวถึงความคืบหน้าในการติดต่อกับบริษัทผู้ผลิตยาทั้งสองชนิด
สำหรับไทม์ไลน์การสั่งซื้อยา Molnupiravir
- ส.ค.-ต.ค.2564 กรมการแพทย์หารือกับบริษัท Merck & Co การจัดหาและการจัดซื้อ รวมถึงสัญญาซื้อขาย
- ต.ค. 2564 เริ่มเสนอแผนการจัดหา ยาดังกล่าวกับ ศบค. และหารือกับอัยการสูงสุด
- พ.ย. 2564 ยื่นต่อคณะรัฐมนตรีเพื่อของบสั่งซื้อยาดังกล่าว คาดการณ์ว่าเป็นช่วงเดียวกับที่ FDA สหรัฐฯ จะอนุมุติยาชนิดนี้ในกรณีฉุกเฉิน
- ตั้งแต่ พ.ย. 2564 – ต้นปี 2565 ขึ้นทะเบียนยาดังกล่าวกับ อย. และใช้ในประเทศไทย
สำหรับไทม์ไลน์ของยา Paxlovid
- ส.ค. 2564 กรมการแพทย์ได้หารือกับบริษัท Pfizer-BioNTech ถึงข้อมูลยาและการวิจัยพัฒนา
- ส.ค.-ก.ย. 2564 Pfizer และกรมการแพทย์ลงนามในเอกสาร CDA เพื่อรักษาความลับไม่เปิดเผยข้อมูล
- ต.ค. 2564 Pfizer และกรมการแพทย์หารือความก้าวหน้าเรื่องงานวิจัยครั้งที่ 2 และครั้งที่ 3
- 12 พ.ย. 2564 หารือความเป็นไปได้ในการจัดหายา คาดว่าจะเป็นช่วงเวลาเดียวกับที่บริษัทขอขึ้นทะเบียนกับ FDA สหรัฐฯ
ต้องถือว่าในการสั่งซื้อยารักษา COVID-19 ครั้งนี้ไทยเราขยับตัวรวดเร็วทีเดียว อย่างไรก็ตาม คงต้องจับตาดูกันต่อไปว่าไทม์ไลน์ที่วางไว้จะสำเร็จลุล่วงด้วยดีหรือเปล่า และข้อตกลงที่ทำร่วมกันจะรัดกุมเพียงพอไหม
เพราะมิฉะนั้นอาจเป็นเหมือนครั้งที่สยามไบโอไซเอนส์ผลิต AstraZeneca ก็เป็นได้
อ้างอิง:
https://www.bbc.com/news/health-59163899